

在光學顯微鏡中,不言而喻燃异,只能從標本被照亮的部分獲得信息携狭。當然,如果照明在空間上不均勻回俐,那么這種不均勻性將使圖像數(shù)據(jù)產(chǎn)生偏差逛腿。然而,照明場的有意進行特殊配置是過去25年中出現(xiàn)的許多提高熒光顯微鏡的空間分辨率技術的基礎仅颇。在文本中单默,我們將介紹固態(tài)光源的輸出特性以及它們?nèi)绾蝹鞑サ匠上駪弥小?/p>
展示全部 
固態(tài)光引擎的空間光輸出特性
1. 固態(tài)光源:激光器和LED
光引擎是一個緊湊的固態(tài)光源陣列,在統(tǒng)一的控制基礎設施下運行灵莲,并饋入統(tǒng)一的光輸出路徑(圖1)雕凹。陣列的元件可以是LED或激光器或兩者的混合殴俱,具體取決于預期應用的要求政冻。在本文中,我們將把激光器的考慮限制在半導體激光器上线欲,半導體激光器的總體尺寸與LED相似明场,允許它們被納入陣列中,而無需從根本上重新設計支持基礎結(jié)構(gòu)李丰。
實際上苦锨,LED和激光器在三個重要方面有所不同:
(1) 光譜分布(圖1)
(2) 光輸出生成效率(圖2)
(3) 輸出空間分布(圖3)。
激光的光譜帶寬較窄(圖1)趴泌,這在熒光顯微鏡中并不特別重要舟舒,因為熒光染料和熒光蛋白的光譜帶寬通常大于LED或激光。相反嗜憔,是輸出空間分布秃励,方便地表示為光學擴展量(étendue)[1],這主要區(qū)分LED和激光器的下游應用吉捶。一般來說夺鲜,光學擴展量是器件的發(fā)光表面積與來自該面積的光的角發(fā)散度的乘積。因此呐舔,激光器的光學擴展量值比LED小得多(表1)币励。這使得LED主要適用于寬視場熒光顯微鏡,主要用于觀察二維樣品珊拼,在較大的視場范圍內(nèi)食呻,其空間分辨率高于衍射極限(>200 nm)。激光器更適用于需要高輻射強度的應用(表1),如共聚焦顯微鏡仅胞,單分子定位顯微鏡和超分辨率顯微鏡浪感。
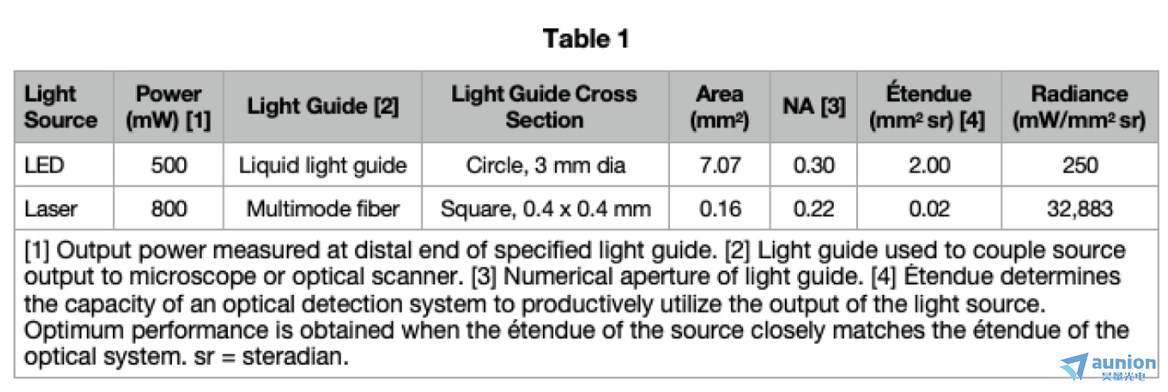
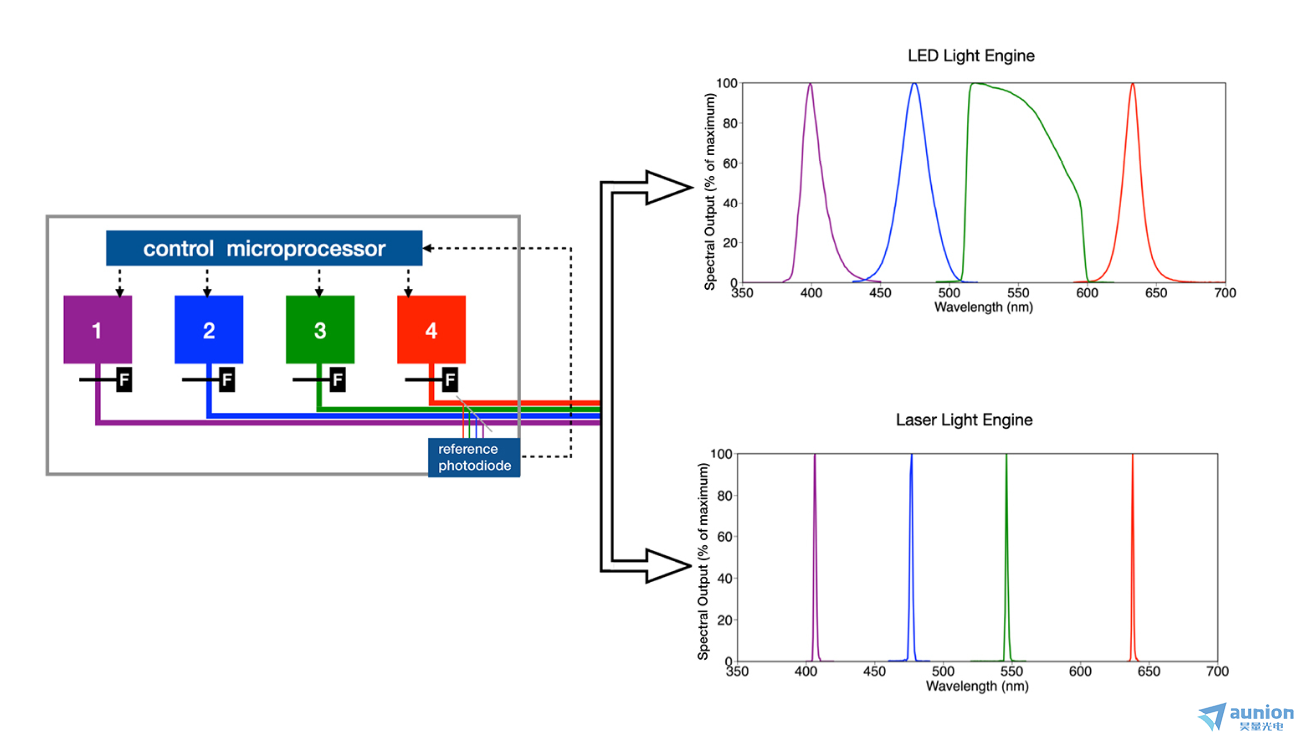
圖1所示。由4個固態(tài)光源陣列組成的光引擎示意圖饼问。在實踐中影兽,根據(jù)應用需求,源的數(shù)量可以在2-21之間莱革。光源可以是LED(產(chǎn)生光譜輸出峻堰,如右上所示)或激光(產(chǎn)生光譜輸出,如右下所示)盅视【杳可以對LED進行濾波(F)以選擇LED光譜輸出的子集。
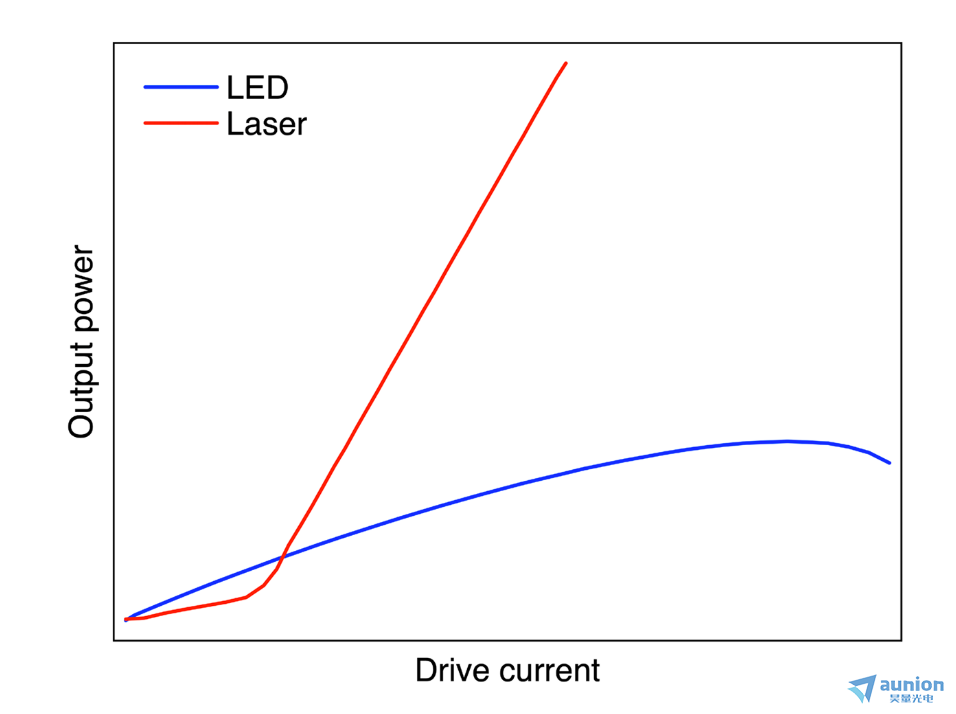
圖2. LED和激光器的光輸出與驅(qū)動電流關系闹击。LED通過半導體的PN結(jié)產(chǎn)生光輸出镶蹋。半導體激光器是類似的,除了光的產(chǎn)生被限制在半導體內(nèi)的一個小腔內(nèi)(圖4)赏半,在那里它被放大贺归,導致在大多數(shù)驅(qū)動電流水平具有更高的輸出功率。
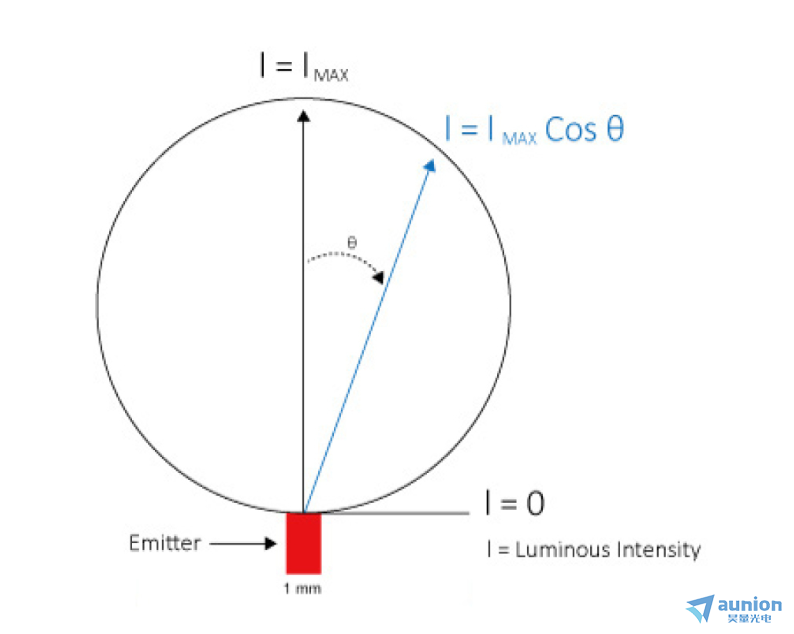
圖3. LED光輸出的朗伯空間分布断箫。熒光顯微鏡應用通常利用光輸出?從0到60°拂酣。
用于熒光顯微鏡應用的單個LED光源通常具有1mm×1mm的發(fā)光表面。從該表面發(fā)出的光具有朗伯空間分布(Lambertian spatial distribution)(見圖3)仲义,這些光必須被準直并z終聚焦以用于顯微鏡婶熬。顯微鏡的光學擴展量限制了可以有效利用的朗伯輸出分布的多少。通常埃撵,這是一個60度半角的錐形赵颅,代表了LED總輸出的大約90%。半導體激光從在多層半導體結(jié)構(gòu)中形成的諧振光學腔中發(fā)出光(見圖4)暂刘。激光二極管的發(fā)光面積大約比LED小4個數(shù)量級(0.0001mm2對比1mm2)饺谬,使其能夠在更小的發(fā)散角內(nèi)提供類似的功率輸出。激光腔的橫向?qū)挾龋òl(fā)射區(qū)寬度鸳惯,見圖4)決定了激光是單模(寬度<10μm)還是多模(寬度>50μm)商蕴。就應用而言,單模和多模半導體激光器在輸出功率和角度發(fā)散之間代表著一種權(quán)衡芝发。
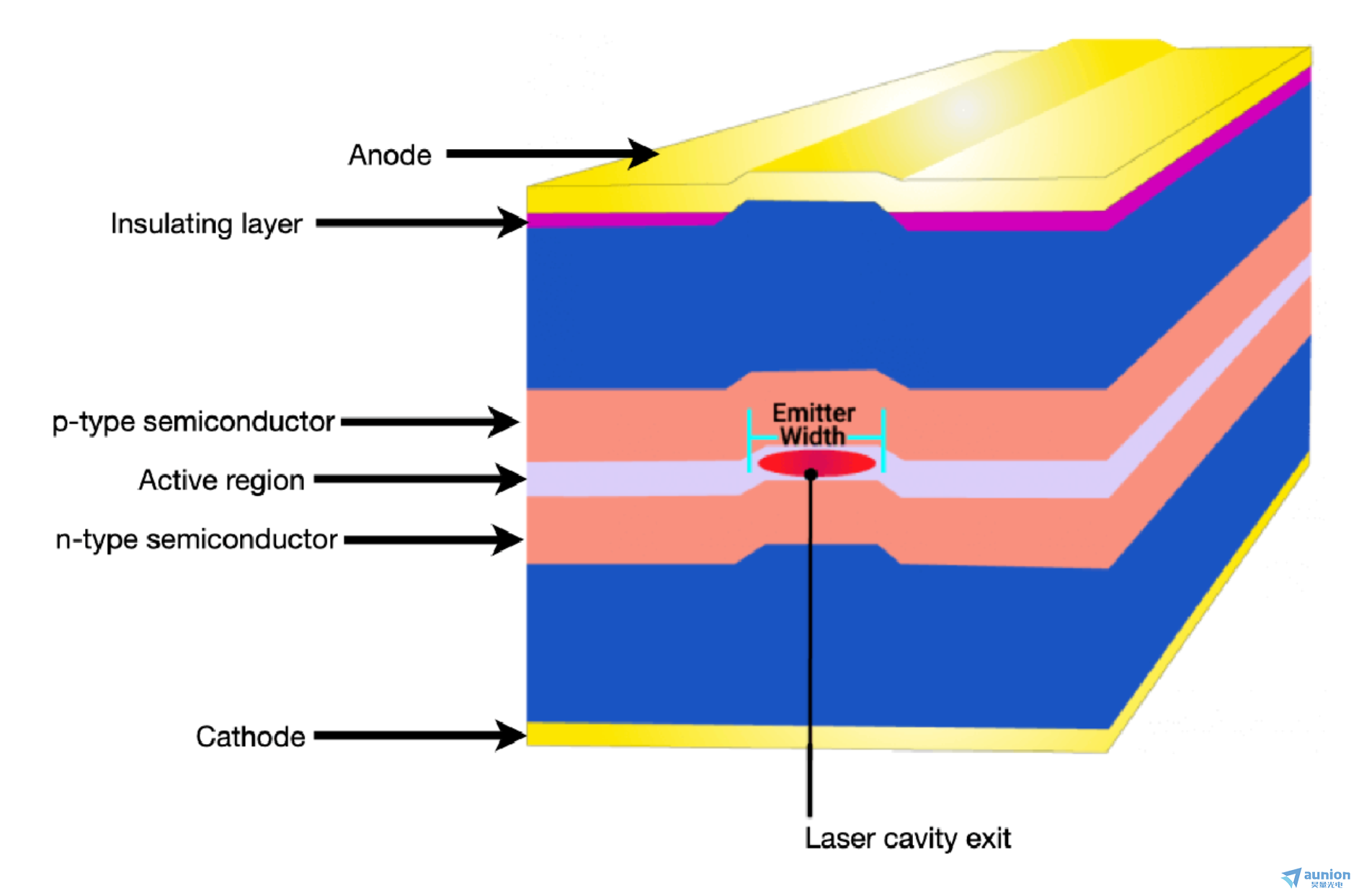
圖4. 法布里-珀羅(FP)半導體激光器示意圖绪商。整機尺寸一般為1000μm×500μm×200μm(長×寬×高)。對于單模激光器辅鲸,發(fā)射區(qū)寬度小于10 μ m格郁,對于高度為1 μ m的多模激光器,發(fā)射區(qū)寬度小于50 μm。
除了高輻射強度和小光學擴展量(見表1)之外例书,激光源的光輸出是相干的锣尉,而LED的光輸出則不是。當激光的相干光被光學粗糙表面反射而隨機化時决采,結(jié)果就會產(chǎn)生激光散斑(見圖5)自沧。在需要均勻照明場的應用中,激光散斑顯然是不利的树瞭。在這種情況下拇厢,可以對激光輸出應用各種技術來擾亂其時間或空間相干性[2]。另一方面晒喷,激光散斑可用于測量表面粗糙度或散射粒子的運動孝偎。這些應用中值得注意的是激光散斑對比成像(LCSI),它用于測量組織中的血液灌注[3]凉敲。

圖5.(左)由ZIVA光引擎(Lumencor, Beaverton, OR)輸出的488nm激光產(chǎn)生的激光散斑圖案衣盾。(右)相同的488nm激光輸出后,通過一個旋轉(zhuǎn)式散斑消除器爷抓。
1. 液體光導(LLG)和光纖輸出
液體光導和光纖提供了從光引擎向下游光學分析系統(tǒng)(如顯微鏡)傳遞光輸出的柔性通道势决。液體光導通常具有比光纖更大的橫截面積和更大的角度接受范圍(數(shù)值孔徑)。因此废赞,光纖通常(盡管不專用于)與激光光引擎配合使用徽龟,而液體光導與LED光引擎配合使用。LED和激光光引擎產(chǎn)生的光的角度分布傳播特性展示在圖6中唉地。圖6(a)顯示了表征方法。根據(jù)光傳輸線出口與投影屏幕之間的已知距離传透,通過相機檢測到的投影輻射光強度值被轉(zhuǎn)換為數(shù)值孔徑(NA)耘沼,通過應用公式NA = n.sinθ。圖6中的數(shù)據(jù)展示了幾個顯著特點朱盐。如預期的那樣群嗤,基于第1節(jié)中描述的特性,通過液體光導傳播的LED光引擎的角度分布比通過多模光纖傳播的激光光引擎的角度分布更寬(比較圖(b)和(c)與圖(d)和(e))兵琳。在圖(d)和(e)中明顯可見的不同激光輻射角度分布差異歸因于源激光的多模輸出狂秘。通過添加下游的光束整形光學元件(圖(f)和(g)),獲得了消色差的角度分布躯肌。這一特性對于使用多色熒光顯微鏡定量確定細胞和組織中分子共定位至關重要[4]者春。
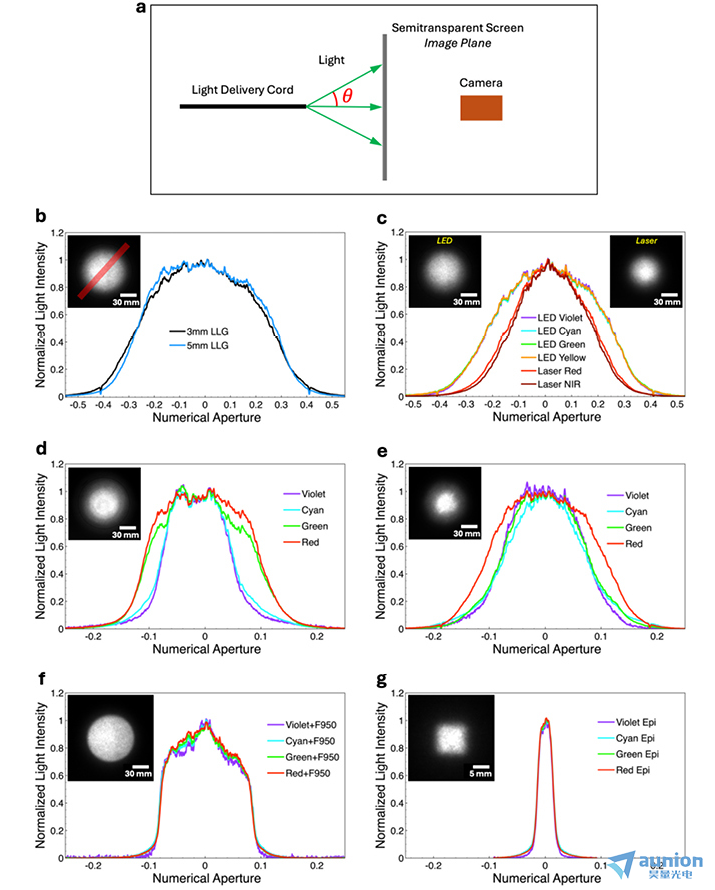
圖6.(a)角度光分布表征方法。通過Thorlabs DCC1240M cmos相機捕捉投影的輻射光分布清女。
(b)由SOLA V-N LED光引擎(Lumencor, Beaverton, OR)產(chǎn)生的未過濾白光(380–760 nm)通過直徑為3毫米或5毫米的液體光導傳輸后的角度分布钱烟。
(c)由多源SPECTRA光引擎(Lumencor, Beaverton, OR)產(chǎn)生的過濾LED和激光光通過直徑為3毫米的液體光導傳輸后的角度分布。紫色LED = 395 nm,青色LED = 475 nm拴袭,綠色LED = 555 nm读第,黃色 = 575 nm,均具有25 nm帶寬拥刻。激光中心波長為637 nm(紅色)和748 nm(近紅外)怜瞒。
(d)由CELESTA光引擎(Lumencor, Beaverton, OR)產(chǎn)生的光通過直徑為1.5毫米(NA = 0.39)的多模光纖傳輸后的角度分布。激光中心波長為405 nm(紫色)般哼、477 nm(青色)盼砍、545 nm(綠色)和639 nm(紅色)。
(e)由CELESTA光引擎(Lumencor, Beaverton, OR)產(chǎn)生的光通過方形0.4毫米×0.4毫米(NA = 0.22)的多模光纖傳輸后的角度分布逝她。激光中心波長為405 nm(紫色)浇坐、477 nm(青色)、545 nm(綠色)和639 nm(紅色)黔宛。
(f)與(e)相同近刘,但光纖遠端的光輸出通過Thorlabs F950多模準直器。
(g)與(e)相同臀晃,但光纖遠端的光輸出通過Lumencor臨界落射照明器(另見圖8)觉渴。
3. 熒光顯微鏡照明
柯勒照明(圖7)自1893年引入以來,一直是寬場落射熒光顯微鏡的主要照明方法[5]徽惋“噶埽柯勒照明開發(fā)的主要動機之一是來自白熾燈燈絲的照明不均勻性,或者是放電燈弧的漂移或閃爍险绘√呔柯勒照明通過將光源置于成像樣本平面的焦點之外(圖7)來消除這些問題。像激光和LED這樣的固態(tài)光源本質(zhì)上更具空間均勻性宦棺,使得實施臨界照明成為可能瓣距,在臨界照明中,光源在圖像平面上聚焦(圖7)代咸。LED提供的柯勒照明在樣本平面上的照射強度為1-100 mW/mm2蹈丸,這對于寬場熒光顯微鏡來說已經(jīng)足夠。然而呐芥,柯勒照明相對效率較低逻杖,因為它并沒有傳播光源發(fā)出的全部面積或全部角度分布的光。對于像單分子定位顯微鏡(SMLM)這樣的特殊成像技術思瘟,需要更高水平的照射強度荸百,大約為10,000 mW/mm2(1 kW/cm2)[6]。這可以通過使用臨界落射照明器實現(xiàn)潮太,該照明器將激光光引擎輸出的超過50%的輸出功率傳遞到樣本平面(圖8)管搪。臨界落射照明器產(chǎn)生均勻的虾攻、高照射強度的照明,其覆蓋面積與用于成像的scmos相機傳感器的面積相匹配更鲁。

圖7. (A)柯勒照明和(B)臨界照明的光學示意圖霎箍。圖A中的垂直虛線表示物鏡的后焦平面。

圖8. 使用CELESTA 光引擎成像的均勻熒光玻璃澡为,該引擎通過800 μm直徑的光纖耦合到安裝在Nikon Ti/Ti 2顯微鏡中的臨界落射照明器漂坏。使用Nikon 60 X/1.4 NA Plan Apo物鏡和Andor Zyla 5.5(2560 x 2160像素)sCMOS相機拍攝圖像。該圖顯示了攝像機沿著標記為紅色的對角線軸記錄的灰度值媒至。右上角的插圖顯示了用Nikon 10 X/0.3 NA Plan Apo物鏡成像的相同樣品顶别。
轉(zhuǎn)盤共聚焦顯微鏡(Spinning Disk Confocal Microscopy, SDCM)利用臨界照明來補償因空間濾波以排除焦平面scmos外光而造成的光通量損失[7]。早期的SDCM實現(xiàn)使用單模激光通過單模光纖耦合到掃描頭(東京橫河電機)拒啰。然而驯绎,這種配置容易出現(xiàn)光學錯位,并且常常在樣本平面上產(chǎn)生不均勻的照明谋旦。通過ZIVA光引擎(Lumencor, Beaverton, OR)實現(xiàn)了顯著改進剩失。ZIVA光引擎整合了七個多模激光源,通過直接電子開關進行波長選擇册着,無需像聲光可調(diào)諧濾波器(Acousto-Optic Tunable filters, AOTFs)這樣的輔助輸出調(diào)制器拴孤。光引擎整合了光束整形和消散斑光學元件,產(chǎn)生與記錄樣本圖像的sCMOS傳感器尺寸布局相匹配的方形照明輪廓(見圖5)甲捏。光輸出通過精密設計的適配器耦合到橫河CSU-W1掃描器演熟,在樣本平面上產(chǎn)生強烈且均勻的照明。通過省略AOTFs和耦合光纖等中間光學元件司顿,提高了光通量芒粹,并且相對于單模激光發(fā)射,減小了系統(tǒng)的尺寸和成本免猾。
全內(nèi)反射顯微鏡(total internal reflection Microscopy, TIRF)通過將熒光激發(fā)限制在樣本平面100 nm范圍內(nèi)是辕,來消除焦平面外光的成像(相比之下, SDCM的z軸分辨率約為500 nm)猎提。TIRF通常通過將激光聚焦到一個非常高數(shù)值孔徑物鏡的后焦平面上的一個約50μm直徑的光斑來實現(xiàn)(“物鏡TIRF”,[8])旁蔼。然而锨苏,通過將LED的輸出通過一個環(huán)形掩模投影到物鏡的后焦平面上,也可以有效地實現(xiàn)TIRF的照明[9]棺聊。物鏡TIRF所需的高放大倍數(shù)物鏡導致視野有限伞租。這一限制可以通過使用波導TIRF來克服,在波導TIRF中限佩,樣本直接放置在高折射率的玻璃蓋片上葵诈,該蓋片通過邊緣耦合連接由LED或激光提供的照明[10]裸弦。
總之,LED和激光在光譜分布作喘、電光轉(zhuǎn)換效率和輸出空間分布方面有著明顯的區(qū)別理疙。其中,空間分布對于定義它們的應用非常重要泞坦。即便如此窖贤,激光應用和LED應用之間存在著相當大的重疊,這得益于能夠在共同的控制和光學基礎設計下容納這兩種類型的光源贰锁。z終赃梧,只有在仔細考慮空間分布的同時,結(jié)合針對分析和成像儀器需求定制的光譜和強度規(guī)格豌熄,才能構(gòu)建出適當?shù)恼彰魇卩郑苑沼诒姸嘈枰庾又С值纳茖W和材料科學應用。
如果您對Lumencor光源有興趣锣险,請訪問上海昊量光電的官方網(wǎng)頁:
http://www.wjjzl.com/three-level-330.html
更多詳情請聯(lián)系昊量光電/歡迎直接聯(lián)系昊量光電
關于昊量光電:
上海昊量光電設備有限公司是光電產(chǎn)品專業(yè)代理商蹄皱,產(chǎn)品包括各類激光器、光電調(diào)制器囱持、光學測量設備夯接、光學元件等,涉及應用涵蓋了材料加工纷妆、光通訊盔几、生物醫(yī)療、科學研究掩幢、國防逊拍、量子光學、生物顯微际邻、物聯(lián)傳感芯丧、激光制造等;可為客戶提供完整的設備安裝世曾,培訓缨恒,硬件開發(fā),軟件開發(fā)轮听,系統(tǒng)集成等服務骗露。
您可以通過我們昊量光電的官方網(wǎng)站www.wjjzl.com了解更多的產(chǎn)品信息,或直接來電咨詢4006-888-532血巍。
參考文獻:
[1] W M?nch (2015) Adv Opt Techn 4:79–85
[2] V Kumar, AK Dubey DS Mehta et al. (2021) Opt Laser Technol 141:107079
[3] W Heeman, W Steenbergen, EC Boerma et al. (2019) J Biomed Opt 24:1–11
[4] J Waters (2009) J Cell Biol 185:1135–1148
[5] A Nolte, JB Pawley L. H?ring (2006) in Handbook of Biological Confocal Microscopy, (3rd Edition), JB Pawley (Ed) pp 126–144
[6] R Diekmann, M Kahnwald, J Rise et al. Nat Methods (2020) 17:909–912
[7] J Oreopoulos, R Berman, M Browne (2014) Methods Cell Biol 123:153–175
[8] A Yildiz, RD Vale (2015) Cold Spring Harb Protoc; doi:10.1101/pdb.top086348
[9] C Suckert, C Zosel, M Schaefer (2024) Cell Calcium 120:102883
[10] S Ramachandran, DA Cohen, R Lal et al. (2013) Sci Rep 3:2133